Etapa tres para ser profesional en galvanoplastia:Concentración correcta del metal y sus efectos en baños ácidos, alcalinos y cianurados
- Gustavo Velez
- hace 2 días
- 3 Min. de lectura
Una vez comprendida la distribución de espesores, el siguiente paso natural en la formación de un profesional en galvanoplastia es dominar la concentración correcta del metal en el electrolito.
La concentración metálica no solo determina la velocidad de deposición; define el régimen electroquímico del proceso, su estabilidad, la eficiencia de corriente y la calidad estructural del recubrimiento.
Un baño puede estar perfectamente formulado en cuanto a aditivos y parámetros eléctricos, pero si la concentración de metal no es la adecuada, el proceso será inestable y poco reproducible.

¿Por qué es crítica la concentración de metal?
Desde el punto de vista del proceso, la concentración del metal controla:
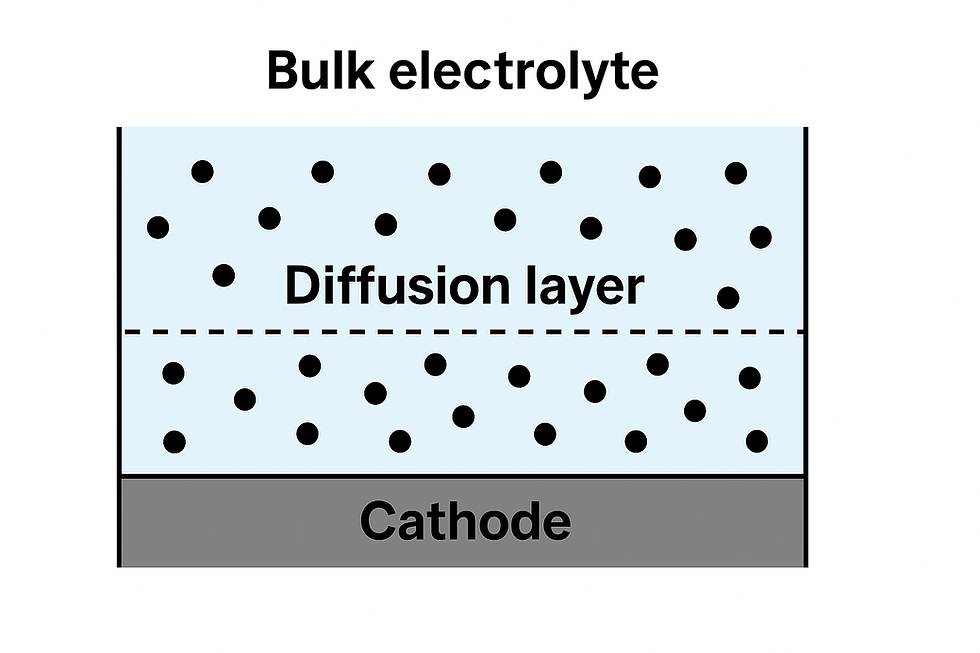
La disponibilidad de iones metálicos en la capa de difusión
El gradiente de concentración en la interfase cátodo–electrolito
El riesgo de operar cerca de la corriente límite por difusión
La competencia entre deposición metálica y reacciones secundarias
En términos prácticos: demasiado poco metal limita el proceso; demasiado metal lo vuelve inestable.
Comportamiento en baños ácidos
En los baños ácidos, el metal se encuentra generalmente libre o débilmente complejado, lo que da lugar a:
Alta velocidad de deposición
Alta eficiencia de corriente
Baja resistencia iónica
🔹 Baja concentración metálica
Cuando la concentración de metal es insuficiente:
La capa de difusión se agota rápidamente
Se alcanza la corriente límite con facilidad
Aparece evolución de hidrógeno
Se generan quemados y depósitos rugosos
Estos efectos se intensifican en zonas de alta densidad de corriente.
🔹 Alta concentración metálica
Un exceso de metal puede:
Incrementar la conductividad de forma no controlada
Aumentar la sensibilidad a variaciones geométricas
Generar depósitos internos con mayor estrés
En baños ácidos, la concentración óptima de metal suele ser un equilibrio fino entre productividad y estabilidad.
Comportamiento en baños alcalinos
En sistemas alcalinos, el metal se encuentra fuertemente complejado (por ejemplo, como zincato u otros complejos).
Esto cambia radicalmente el comportamiento del proceso.
🔹 Baja concentración metálica
Se reduce la velocidad de deposición
La eficiencia de corriente cae
El proceso se vuelve muy sensible a densidad de corriente
Aunque la distribución de espesores puede mantenerse aceptable, el proceso pierde productividad.
🔹 Alta concentración metálica
Se rompe el equilibrio del complejo
Aumenta el riesgo de depósitos opacos o grisáceos
Puede aparecer metal químicamente precipitado
En baños alcalinos, la ventana operativa de concentración metálica es más estrecha y requiere control analítico riguroso.
Comportamiento en baños cianurados
Los sistemas cianurados representan el caso más controlado desde el punto de vista electroquímico.
El metal se encuentra altamente complejado, lo que genera:
Baja concentración de ion libre
Alta resistencia al paso de corriente
Excelente capacidad de redistribución de corriente
🔹 Baja concentración metálica
Muy buena penetración
Excelente uniformidad de espesores
Menor velocidad de deposición
🔹 Alta concentración metálica
Se pierde parte del efecto regulador del complejo
Se incrementa el consumo de corriente
Aparecen defectos superficiales
Históricamente, estos sistemas demostraron que la estabilidad del proceso es inversamente proporcional a la fracción de metal libre.
Relación con densidad de corriente
La concentración de metal nunca debe analizarse de forma aislada. Siempre debe evaluarse junto con la densidad de corriente real de operación.
Alta densidad + baja concentración = agotamiento de la capa de difusión
Baja densidad + alta concentración = deposición ineficiente y estrés interno
Un proceso profesional ajusta la concentración metálica en función del rango de densidad de corriente, no solo de un valor nominal.
Influencia de la agitación y temperatura
Agitación: a mayor flujo, mayor capacidad del baño para soportar concentraciones metálicas más bajas sin agotamiento local.
Temperatura: incrementa solubilidad, movilidad iónica y estabilidad del complejo metálico.
Esto significa que el mismo baño puede requerir diferentes concentraciones metálicas según su hidrodinámica y temperatura de operación.
Otros factores que interactúan con la concentración metálica
Tipo y nivel de aditivos orgánicos
Geometría de las piezas
Relación anódica/catódica
Tipo de rectificación (continua, pulsada)
En un sistema bien diseñado, la concentración metálica se convierte en una variable de ajuste fino, no en una constante rígida.
¿Cómo lograr y mantener la concentración correcta?
Un enfoque profesional incluye:
Análisis químico periódico y confiable
Reposición de metal basada en consumo real, no en estimación
Ajustes coordinados con densidad de corriente y producción
Registro histórico del comportamiento del baño
La concentración correcta no se define una sola vez: se mantiene activamente.
Conclusión
La concentración del metal es uno de los pilares invisibles del control en galvanoplastia. Define la frontera entre un proceso reactivo y uno verdaderamente ingenierizado.
Comprender su comportamiento en baños ácidos, alcalinos y cianurados permite anticipar problemas, mejorar estabilidad y elevar la calidad del recubrimiento de manera consistente.
En la galvanoplastia profesional, el metal en solución no solo se deposita:se administra con criterio técnico.


Comentarios